每日經濟新聞 2023-05-12 21:20:54
◎清華大學藥學院藥品監管科學研究院院長楊悅提到,應該從累積凈現值(各年度凈現金流量的合計)來評估創新藥,現在創新藥進入醫保速度平均為1年左右,醫保談判縮短了藥物的市場獨占期,應考慮給予早期產品價格保護。
◎2016年以前,國產創新藥的上市申請(NDA)和獲批數量都是個位數,2016年開始,境內申請人在研新藥IND申請和獲批數量已超越境外申請人。
每經記者 金喆 每經編輯 魏官紅
隨著越來越多的國產創新藥獲批上市,一年一度的醫保談判備受外界關注。
“十年磨一劍”的創新藥要不要降價,是很多生物制藥公司在商業化道路上頗為糾結的問題。
5月11日,清華大學藥學院藥品監管科學研究院院長楊悅在第三屆紅杉全球醫療健康產業峰會上表示,2015年藥品審評審批制度改革以來,中國的創新藥蓬勃發展,改變了以往以仿制藥為主的研發和產業發展的邏輯,向著原始創新的方向發展。
她同時提到,應該從累積凈現值(各年度凈現金流量的合計)來評估創新藥,現在創新藥進入醫保速度平均為1年左右,醫保談判縮短了藥物的市場獨占期,應考慮給予早期產品價格保護。
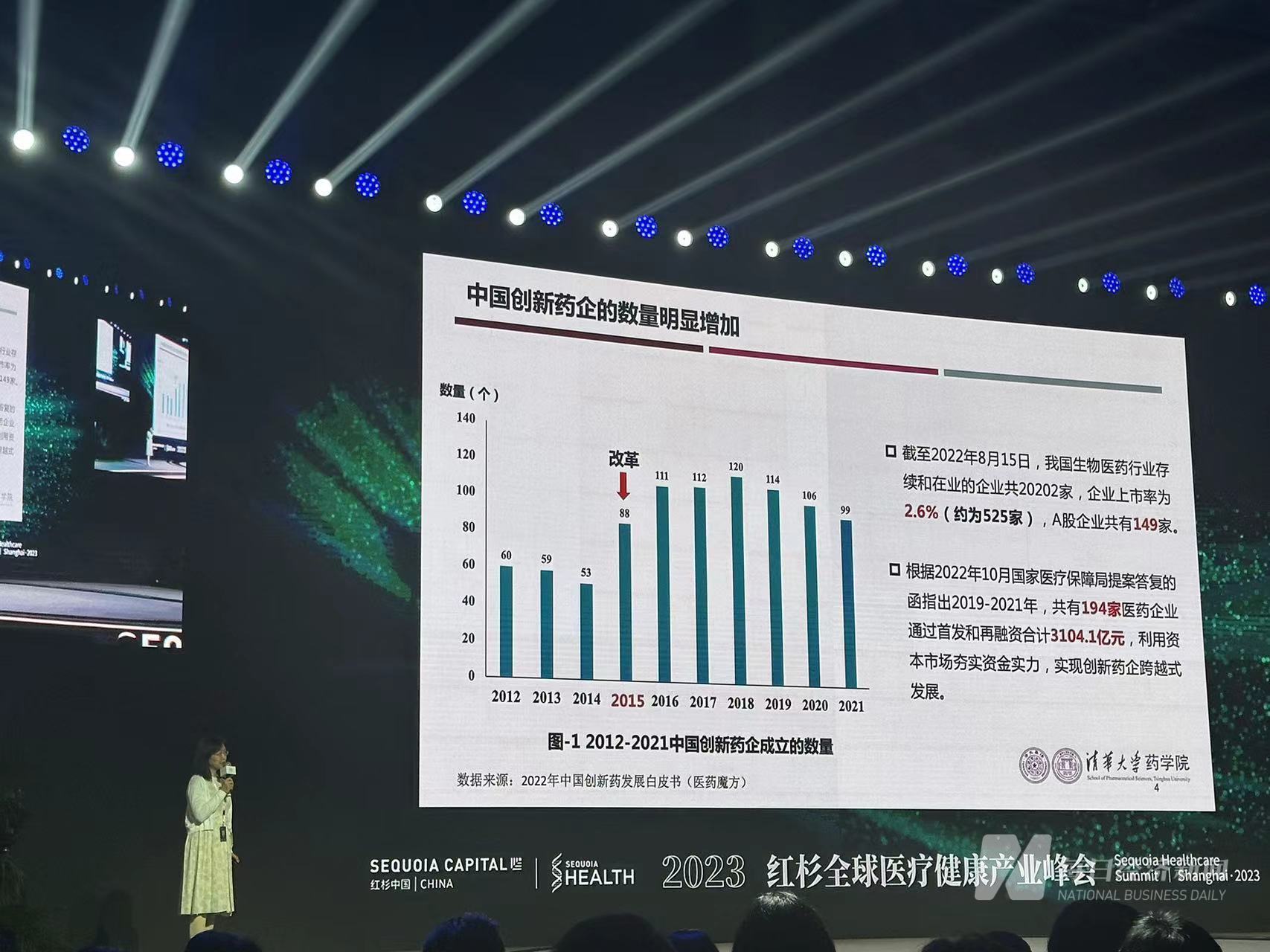
“從很多數據上能看到,每年新增的創新企業數量基本在百家以上。”楊悅提供的數據顯示,截至2022年8月15日,中國生物醫藥行業存續和在業的企業共20202家,企業上市率為2.6%(約為525家),其中A股企業共有149家。
圖片來源:每經記者 金喆 攝
2022年10月國家醫保局提案答復的函指出,2019年-20221年,共有194家醫藥企業通過首發和再融資合計3104.1億元,利用資本市場夯實資金實力,實現創新藥企跨越式發展。
另外,從歷年申請臨床研究(IND)和上市申請(NDA)數量變化,也能看出我國藥品審評審批的成果。2016年以前,國產創新藥的上市申請(NDA)和獲批數量都是個位數,2016年開始,境內申請人在研新藥IND申請和獲批數量已超越境外申請人。
《每日經濟新聞》記者在現場了解到,一組數據能見證中國創新藥企業近年的成長——2014年,中國入榜研究與試驗發展(R&D)全球2500強的醫藥與生物制藥企業只有19家,2021年入榜企業數量已達到65家,其中2家進入醫藥與生物制造領域前50。
創新藥研發是醫藥行業公認的“燒錢”賽道,受益于我國創新藥的蓬勃發展,近年來醫藥研發投入不斷攀升。國家統計局、科學技術部和財政部聯合公布的《2021年全國科技經費投入統計公報》顯示,醫藥制造業的研究與試驗發展(R&D)經費投入和投入強度分別為942.4億元和3.19%,分別是制造業的第六名和第三名。
據不完全統計,2022年,醫藥生物行業上市公司研發投入同比增長15.04%,達到1179.27億元。盡管如此,中國的醫藥生物公司與美國相比還有較大差距,美國占全球創新藥市場的50%以上,我國大部分上市的創新藥產品還沒有在海外摘果子。
楊悅提出,中國藥企排名不斷上升,比如百濟神州2021年在榜單中的排名為第150位(2020年為209位),一年時間提升59位。但與跨國藥企排名相比差距明顯,正在加速追趕。記者注意到,在上述榜單的TOP50和TOP100名單中,美國企業分別有約20家、45家,但2019年以前中國沒有企業進入TOP50,不到5家企業入圍TOP100。
醫藥企業在研發端的紅火場面,也讓創新藥近年來陸續進入收獲期。2021年,國家藥監局共批準32款創新藥(化藥和治療用生物制品)上市,2022年批準超40款。越來越多國產創新藥獲批上市,而每年底舉行的醫保談判備受外界關注。
從目前情況來看,創新藥物上市后大概一年半時間之內就能迎來進入醫保的機會,每年談判成功的品種,進入醫保的平均時間間隔不斷縮短。
國家醫保局醫藥服務管理司副司長黃心宇此前接受媒體采訪時介紹,2022年醫保目錄調整主要面向5年內新上市或修改說明書的藥品、新冠感染治療用藥、國家基本藥物、罕見病用藥等。本次目錄新增的藥品大部分是5年內新上市的藥品。調整中,共有24個國產重大創新藥品被納入談判,最終奧雷巴替尼等20個藥品談判成功,成功率達83.3%。
與此同時,創新藥的價格也在醫保談判后大幅下降。記者注意到,國內藥企一直在呼吁給予創新藥更高的價值空間。今年兩會期間,第十四屆全國人大代表、榮昌生物董事長王威東擬提交關于提高創新藥可及性和促進創新藥企產業化的建議。
他提出兩點建議,一、創新談判藥品評估體系,實施定價保護機制。對臨床價值高、患者急需、替代性不強的創新藥,特別是同類首創、同類最佳的藥品,給予企業進入醫保目錄后5-8年的價格保護期,新增適應癥也以“零降價”方式進入醫保目錄,便于收回研發成本,保護新藥研發及開拓新適應癥的積極性。
二、將談判藥品進入醫保目錄的協議期延長至5年以上。目前兩年的協議有效期不能滿足創新藥市場準入的周期要求,兩年協議期滿后又將面臨再次談判及降價,程序繁瑣且影響創新藥的可及性。
在5月11日的峰會上,楊悅表示,新藥獲得批準后的一段時間內,該藥物的生產和銷售由持有相關專利的公司獨家擁有。“獨占期”與臨床試驗管理、激勵政策、未來區分價值等幾個方面,其中激勵政策決定了(記者注:藥品銷售周期)曲線的平緩還是陡峭,迅速往上去就獲利了,但現在創新藥一談判,價格可能很快就下去,相當于“獨占期”提前到來,因此要完善創新藥的國家醫保準入制度。
她提到,對產業來說,以“獨占期”為核心的拉動型激勵是最大的激勵,各個國家對創新藥的“獨占期”有差異化設計,美國鼓勵的是原始創新,歐盟、日韓鼓勵的是改良型創新。現在我國已經把數據保護的相關內容寫進征求意見,會對創新藥產業或創新藥的研發產生第二次重要的再激勵。
如需轉載請與《每日經濟新聞》報社聯系。
未經《每日經濟新聞》報社授權,嚴禁轉載或鏡像,違者必究。
讀者熱線:4008890008
特別提醒:如果我們使用了您的圖片,請作者與本站聯系索取稿酬。如您不希望作品出現在本站,可聯系我們要求撤下您的作品。
歡迎關注每日經濟新聞APP
